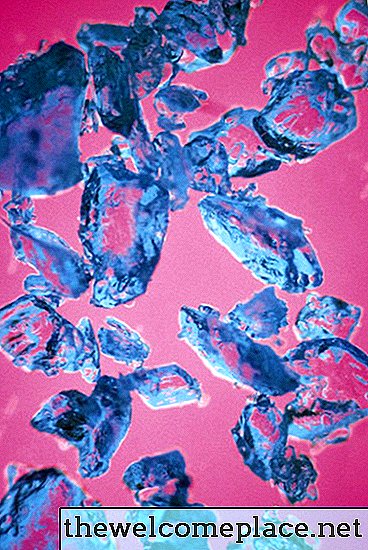
Podobnie jak wiele kompleksów metali przejściowych, pięciowodny siarczan miedzi (II) ma jaskrawe zabarwienie; kryształy tej pięknej substancji mają jasny odcień niebieskiego. Jego kolor wynika z chemii i fizyki jego składu - a ściślej z rodzaju wiązań, jakie tworzy z jonami siarczanowymi i cząsteczkami wody przyłączonymi do miedzi.
 Pentahydrat siarczanu miedzi ma piękny półprzezroczysty niebieski kolor.
Pentahydrat siarczanu miedzi ma piękny półprzezroczysty niebieski kolor.Orbitale
Elektrony wykazują dualizm falowo-cząsteczkowy, co oznacza, że mają zarówno właściwości podobne do fali, jak i podobne do cząstek. Zachowanie elektronu w atomie opisuje równanie falowe zwane funkcją falową. Kwadrat funkcji falowej daje prawdopodobieństwo znalezienia elektronu w dowolnym punkcie w danym momencie. Funkcje falowe elektronów w atomach są również nazywane orbitalami atomowymi. Chemicy nazywają orbitale atomowe za pomocą liczby oznaczającej poziom energii orbity, po której następuje litera oznaczająca rodzaj orbity. W przypadku elementów w czwartym okresie układu okresowego lub wyższych, musisz skupić się tylko na trzech rodzajach orbitali, mianowicie s, pid. Aby poznać kształt tych orbitali, zobacz link w sekcji zasobów.
Podział pola krystalicznego
Jon miedzi w siarczanie miedzi (II) utracił dwa elektrony, więc ma ładunek +2. Ma dziewięć elektronów w swoim najbardziej zewnętrznym poziomie energii lub powłoce; te tak zwane elektrony walencyjne zajmują orbitale 3d. Cząsteczki wody i jony siarczanowe są przyciągane przez dodatni ładunek jonu miedzi, więc zbliżają się do niego i układają wokół niego w konfiguracji oktaedrycznej. W konsekwencji dwa z pięciu 3d orbitali jonu miedzi wyrównują się wzdłuż osi, do których zbliżają się jony siarczanowe i cząsteczki wody; ponieważ zarówno elektrony na tych orbitaliach, jak i elektrony w cząsteczkach / jonach mają ładunek ujemny, odpychają się nawzajem. Ostatecznie zatem dwie z pięciu 3d orbitali mają zwiększoną energię; nazywane są one np. orbitaliami. Natomiast pozostałe trzy mają zmniejszoną energię i są nazywane orbitalami t2g.
Absorpcja światła
Foton światła zostanie pochłonięty przez kompleks koordynacyjny, jeśli ma energię równoważną różnicy między stanem, w którym obecnie przebywa elektron, a dostępną mu energią innego stanu. W konsekwencji kompleks siarczanu miedzi może pochłaniać fotony światła o energiach równoważnych różnicy energii między t2g a np. Orbitaliami. Tak się składa, że różnica energii dla kompleksu siarczanu miedzi jest równoważna różnicy energii dla fotonów światła w czerwono-pomarańczowym obszarze widma. Ponieważ światło czerwonawe jest pochłaniane podczas przesyłania światła niebieskiego, siarczan miedzi wydaje się niebieski.
Rozpuszczanie w wodzie
Gdy siarczan miedzi rozpuszcza się w wodzie, jony miedzi i siarczanu ulegają dysocjacji. Teraz jon miedzi tworzy ośmiościenny kompleks, w którym jest otoczony sześcioma cząsteczkami wody. Efekt jest jednak nadal taki sam, ponieważ podział na orbitale t2g i np. Orbitale w tym nowym kompleksie jest nadal taki, że światło czerwonawo-pomarańczowe jest pochłaniane i widać roztwór w kolorze niebieskim.